���ǰ���������Ʈ | ������ ���ڡ� �� ���迡�� �ڷγ�19 ����� �ż��� ������ �����ǰ� ������, �پ��� ��� �÷��� ����� ���ǰ� �ִ�. �̷��� ��� ��ǰ�Ǿ�ǰ����ó�� �ڷγ�19 ����� Ư¡�� �ۿ������ ���� �����ߴ�.
‘��� �÷���’�̶� ��ſ��� Ư�� ���̳� �������� � �ٲپ� ����� �����ϴ� ��� �����, �̸� Ȱ���ϸ� ��� ���� �Ⱓ�� ũ�� ������ �� �ִ�.
�̷��� ��� �÷������� ����̷������� ��� ��RNA ��� �������� ��� ���Ȱȭ ��� ���� �ִ�.
��� ������ ���� �ڷγ�19 ��������� ������ ����.
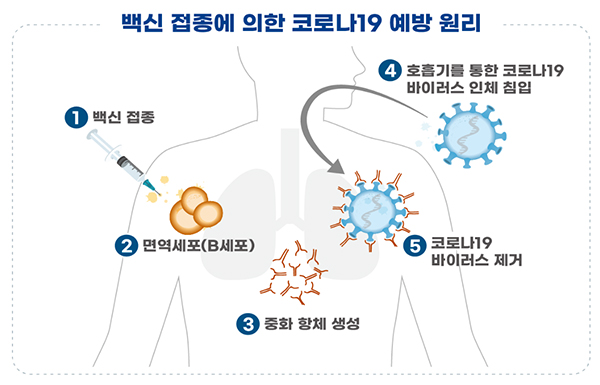 |
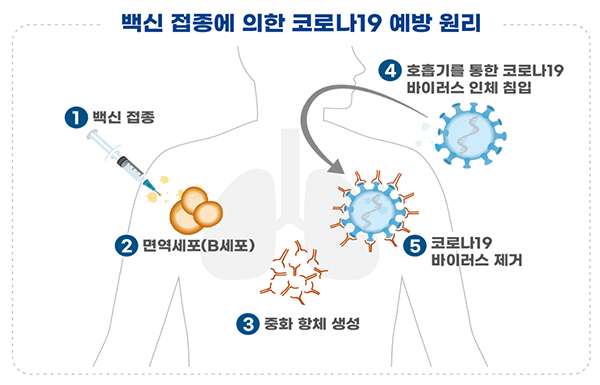
| �� ��� ������ ���� �ڷγ�19 ���� ����. (����= �ľ�ó) |
➊ �ڷγ�19 ����� �����´�.
➋ ��ü ���� ���� ����� �� ���е��� �鿪����(B ����)�� �ڱؽ�Ų��.
➌ �ڱص� B �������� ���̷����� ������ �� �ִ� ��ȭ��ü�� ���� ���ӿ� �����ϰ� �ִ´�.
➍ �ڷγ�19 ���̷����� ȣ���⸦ ���� ħ���ϴ� ���,
➎ ������ ��ȭ��ü�� ħ���� �ڷγ�19 ���̷����� �����Ѵ�.
���̷������� ����� �� �����ڸ� ��ü�� ������ �Ƶ�����̷��� �� �ٸ� ���̷��� ������ ������ ü������ �� �ܹ����� ���������ν� �鿪������ �����ϴ� ����̴�. ��ǥ������ �ƽ�Ʈ������ī ���, �Ἶ ��� ���� �ִ�. �̵��� ��� �ѱ��� ������ �����̴�.
���� ��ƽ�Ʈ������ī ����� ħ�������Ը� �����Ǵ� �Ƶ�����̷����� ����ü�� ����Ѵ�. RNA ��ſ� ���� ��������� ���� �������� Ư¡�� �ִ�. ���� ����ִ� �Ƶ�����̷����� ����ϹǷ� �����(4��)�� ���ϴ� �ݵ�ü���� �ʿ��ϴ�.
�ƽ�Ʈ������ī ����� �������� ���� 12�� 30�� ���� ������ �ߴ�. �����Ǿ�ǰû(EMA)�� ������ 10������ �������並 �����ϰ� �ִٰ� �˷��� �ִ�. ���������� �㰡 ��û(2021.1.4.)�Ǿ� ���� �ľ�ó�� ǰ���㰡 �ɻ� ���̴�.
�� ������� �㰡�� ������δ� �Ἶ���� ������ ����� �ִ�.
��Ἶ ����� ������ 9������ 3�� �ӻ������ ���� ���̴�. ������� �ؿ� �㰡���� ��ʴ� ����. ���������� ���ӻ�·ǰ�� �ڷῡ ���� �������䰡 ��û(2020.12.22.)�Ǿ� ���� ���� ���̴�.
���� ���߷δ� �㼿���� ����� �ӻ� 1/2���� ���� ���̴�.
RNA ����� �� �����ڸ� RNA ���·� ������ ü������ �� �ܹ����� ������ �鿪������ �����ϴ� ����̴�. ��ǥ������ ȭ���� ���, ����� ��� ���� ������ �ѱ��� ���� �����̴�.
�̵��� ���� �Ⱓ�� ª�� �ż��ϰ� �ܱⰣ ���� �뷮������ �����ϳ�, RNA ����ȿ��(RNase)�� ���� �ּ����� RNA�� ���صǾ� �������� ���� �ʾ� �õ�((��) -20�� �Ǵ� –75±15��)�� �ݵ�ü�� �ʿ��ϴ�. �� ������δ� �ڷγ�19 ����� ó������ ��ǰȭ �Ǿ���.
��ȭ���� ����� ���� ���� ������ ������ ����(2020.12.02.), �̱�(2020.12.11.), ij����(2020.12.09.) ���� �ִ�. ������(2020.12.19.) �� ����(EU)(2020.12.21.)������ ���Ǻ� �㰡�ߴ�.
���躸�DZⱸ(WHO)�� ���� ����(2020.12.31.)�Ͽ� �� ���������� ȭ���� ����� ����ϰ� �ִ� ��, ���������� ���� �����ϴٴ� �������� �ǹ̰� �ִ�.
���������� ���ӻ�·�ӻ� �ڷῡ ���� �������䰡 ��û(2020.12.18.)�Ǿ� ���� ���� ���̴�.
����� ����� �̱�(2020.12.18.)���� ���� ������ �߰�, ����(EU)(2021.1.6.)������ ���Ǻ� �㰡�ߴ�. �������� �������� �� ǰ���㰡 ��û ���̴�.
���� ���� ������δ� RNA ��Ű� ������ ������ DNA ����� ���ؽŰ� �����������п��� ���� ���� ���̸� �ӻ� 1/2�� ���� ���̴�.
�ڷγ�19 ������δ� ��ٹ齺 ����� ������, ������ 9������ 3�� �ӻ������ ���� ���̴�. ������� �ؿ� �㰡���� ��ʴ� ����. ���� ���߷δ� SK���̿����̾� ����� �ӻ� 1/2�� ���� ���̴�.
�ľ�ó ���� "�ڷγ�19 ��ſ� ���� ������ ������ ���� ���� ������ ����� ������·��ȿ�� ������ ����ؼ� �����ϰ� �츮 ������ �Ƚ��ϰ� ����� �������� �� �ִ� ȯ���� ����� �� ����ϰڴ�"�� ���ߴ�.
 |
| ���ڷγ�19 ��Ű��� �÷��� ����. (����= �ľ�ó) |
➊ (���̷������� ���) �ڷγ�19 ���̷����� ǥ���� �����ڸ� �ٸ� ���̷���(�Ƶ�����̷��� ��) ������ �־� ������ ü������ ǥ���� �ܹ����� ���������ν� �鿪���� ����
�� : �ƽ�Ʈ������ī��(����), �Ἶ��(�̱�)
➋ (��Ȱȭ ���) ����Ų �ڷγ�19 ���̷����� ü�� ������ �鿪���� ����
�� : �ó�����(�߱�)
➌ (DNA ���) �ڷγ�19 ���̷����� ǥ���� ������(DNA)�� ������ ü������ ǥ���� �ܹ����� ������ �鿪���� ����
�� : �̳�����(�̱�)
➍ (RNA ���) �ڷγ�19 ���̷����� ǥ���� �����ڸ� RNA ���·� ������ ü������ ǥ���� �ܹ����� ������ �鿪���� ����
�� : ȭ������(�̱�), �������(�̱�)
➎ (������ ���) ������������ ����� �̿��� ���� �ڷγ�19 ���̷����� ǥ���� �ܹ����� ���� �����Ͽ� �鿪���� ����
�� : ��ٹ齺��(�̱�)
➏ (���̷��� �������� ���) �ڷγ�19 ���̷��� ǥ���� �ܹ����� ���̷����� ������ ���� ������� ����� �����Ͽ� �鿪���� ����
�� : �ε� ��û������
������ ���� kunkang1983@naver.com
<���۱��� © �ǰ���������Ʈ ���ͳ���, ���� ���� �� ����� ����>
#�ľ�ó#��ǰ�Ǿ�ǰ����ó#���#�ڷγ�#�ǰ���������Ʈ

![[4�� Ư��] �� ���� �ߺ����� ���ϰԡ���� �� �����](/news/photo/202404/39838_32395_2841.jpg) [4�� Ư��] �� ���� �ߺ����� ���ϰԡ���� �� �����
[4�� Ư��] �� ���� �ߺ����� ���ϰԡ���� �� �����
![[�豤���� ġ�ƽ�ũ��] �Ƹ��� �Ҹ��� ��Ÿ��� ����](/news/thumbnail/202404/39860_32421_4530_v150.jpg)