ЁМАЧАДйРЬСІНКЦЎ | УжЙЮПЕ БтРкЁН
GCГьНЪРкМП(031390, РЬЕцСж)РК ЙЬБЙ FDAЗЮКЮХЭ РЬЙУМП-ПЄООПЁ ДыЧб УщРхОЯ ШёБЭРЧОрЧА СіСЄРЛ НТРЮ ЙоОвДйАэ 12РЯ ЙрЧћДй.
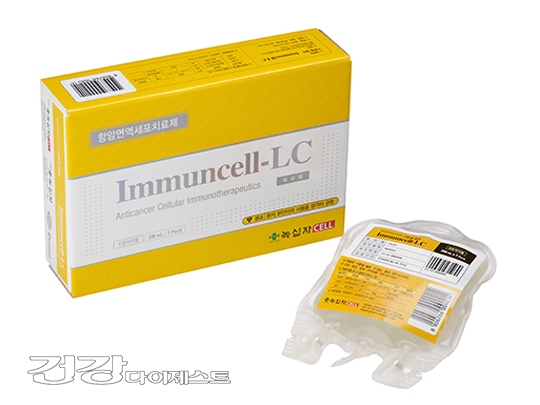 |
РЬЙУМП-ПЄООДТ БЙГЛПЁМ 2007Гт НФЧАРЧОрЧАОШРќУГРЧ ЧАИёЧуАЁИІ ШЙЕцЧЯПЉ Л§Лъ Йз ЦЧИХСпРЮ ИщПЊЧзОЯСІЗЮ ЙЬБЙ НФЧАРЧОрБЙ(FDA)ПЁМ 6Пљ АЃОЯ, 8Пљ ГњСООч(БГИ№ММЦїСО)ПЁ ДыЧб ШёБЭРЧОрЧАРИЗЮ СіСЄЕШ ЕЅ РЬОю ММ ЙјТАЗЮ СіСЄЙоОвДй.
УщРхОЯ ПЌБИРкСжЕЕ РгЛѓНУЧшРК 2009ГтКЮХЭ ПЌММДы ММКъЖѕНККДПјПЁМ СјЧрМК УщРхОЯ ШЏРкПЁАд РЬЙУМП-ПЄООИІ 10ШИ ХѕПЉЧЯПЉ ЦђБе 25%РЧ ФЁЗс ЙнРРЗќРЛ ШЎРЮЧЯПДДй. GCГьНЪРкМПРК 2014Гт 6Пљ SCIРњГЮРЮ ‘ОЯ ИщПЊЧа·ИщПЊФЁЗс’ПЁ СјЧрМК УщРхОЯ ШЏРкИІ ДыЛѓРИЗЮ Чб РЬЙУМП-ПЄОО ПЌБИРкСжЕЕ РгЛѓНУЧш АсАњИІ ЙпЧЅЧпДй.
FDAРЧ ШёБЭРЧОрЧА СіСЄ(ODD, Orphan Drug Designation)РК ШёБЭГФЁМК СњКД ЖЧДТ Л§ИэРЛ РЇЧљЧЯДТ СњКДРЧ ФЁЗсСІ АГЙп Йз ЧуАЁАЁ ПјШАЧЯАд РЬЗяСњ Мі РжЕЕЗЯ СіПјЧЯДТ СІЕЕРЬДй. ШёБЭРЧОрЧАРИЗЮ СіСЄЕШ ФЁЗсСІДТ ММБн АЈИщ, НХОрНТРЮ НЩЛчКёПы ИщСІ, НУЦЧЧуАЁ НТРЮ ШФ 7ГтАЃ ЕЖСЁБЧ РЮСЄ Ею ДйОчЧб Ч§ХУРЬ КЮПЉЕШДй.
GCГьНЪРкМП РЬЕцСж ЛчРхРК “РЬЙУМП-ПЄООРЧ FDA ШёБЭРЧОрЧА СіСЄРЛ ХыЧи ЙЬБЙ РгЛѓНУЧш Йз ЧуАЁАњСЄРЛ АЃМвШЧЯПЉ НУАЃАњ КёПы Р§АЈШПАњИІ БтДыЧЯАэ РжДй. ЧіРчБюСі ШёБЭРЧОрЧАРИЗЮ СіСЄ ЙоРК АЃОЯ, ГњСООчАњ ДѕКвОю УщРхОЯ НУРхПЁМЕЕ ЙЬБЙ СјУтРќЗЋРЛ БИЛѓЧЯПЉ Л§ЙАРЧОрЧА ЧуАЁНХУЛ(BLA)РЛ РЏИЎЧЯАд СЂБйЧв АшШЙРЬДй”Аэ ЦїКЮИІ ЙрЧћДй.
GCГьНЪРкМПРК FDA ШёБЭРЧОрЧА СіСЄРЛ АшБтЗЮ МКАјРћРЮ ЙЬБЙ НУРх СјУтРЛ УпСјЧбДйАэ ОЫЗШДй. АќАшРк УјРК "БЙГЛПЁМДТ МП МОХЭ НХУрРЛ ХыЧи Л§ЛъНУМГ ШЎУц Йз ТїММДы ММЦїФЁЗсСІ CAR-T Ею НХСІЧА АГЙпРЛ РЇЧб РЮЧСЖѓ БИУрАњ ММЦїФЁЗсСІ БлЗЮЙњ СјУтРЛ РЇЧб МКРхЕПЗТРЛ ШЎКИЧЯАэ РжДй"Аэ РќЧпДй. МП МОХЭДТ 2019Гт ИЛ GMPРЮСѕРЛ ИёЧЅЗЮ ЧЯАэ РжДй.
УжЙЮПЕ БтРк kunkang1983@naver.com
<РњРлБЧРк © АЧАДйРЬСІНКЦЎ РЮХЭГнЦЧ, ЙЋДм РќРч Йз РчЙшЦї БнСі>


![[4Пљ ЦЏС§] ГЛ ИіПЁ ЙпКйРЬСі ИјЧЯАдЁІСЖБтПЁ ОЯ ПЙЙцЙ§](/news/photo/202404/39838_32395_2841.jpg) [4Пљ ЦЏС§] ГЛ ИіПЁ ЙпКйРЬСі ИјЧЯАдЁІСЖБтПЁ ОЯ ПЙЙцЙ§
[4Пљ ЦЏС§] ГЛ ИіПЁ ЙпКйРЬСі ИјЧЯАдЁІСЖБтПЁ ОЯ ПЙЙцЙ§
![[БшБЄМіРЧ ФЁОЦНУХЉИД] ОЦИЛАЈ МвИъРЬ ОШХИБюПю РЬРЏ](/news/thumbnail/202404/39860_32421_4530_v150.jpg)